ОБНАРУЖЕН РЕАЛИСТИЧНЫЙ СПОСОБ ПРИСОЕДИНЕНИЯ АМИНОКИСЛОТ К РНК БЕЗ ПОМОЩИ ФЕРМЕНТОВ И РИБОЗИМОВ
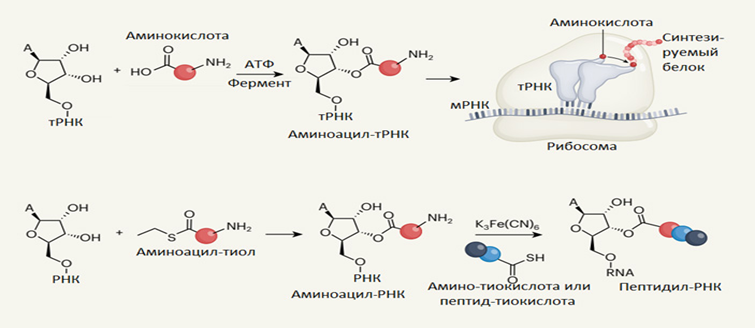
Британские химики обнаружили простой, эффективный и «пребиотически правдоподобный» способ неферментативного аминоацилирования РНК, то есть присоединения аминокислот к РНК без помощи сложных катализаторов, таких как белковые ферменты или рибозимы. Исследование показало, что аминоацил-тиолы избирательно реагируют с двухцепочечными РНК в водном растворе, почти не вступая в другие реакции и не давая ненужных побочных продуктов. В результате аминокислота аккуратно присоединяется как раз к тому месту молекулы РНК, к которому ее присоединяют ферменты аминоацил-тРНК-синтетазы в ходе аминоацилирования транспортных РНК — ключевого этапа синтеза белка в живых клетках. Исследователи также показали возможность абиогенного синтеза аминоацил-тиолов в правдоподобных условиях. Открытие показало вероятные первые шаги в эволюции программируемого синтеза белка — главного эволюционного достижения РНК-мира. Появление программируемого рибосомного синтеза белков— важнейшее эволюционное событие, открывшее перед примитивными репликаторами РНК-мира небывалые возможности и обеспечившее успех всего удивительного предприятия под названием «земная жизнь». Расшифровка деталей этого события — сложная и увлекательная научная задача, над которой ученые небезуспешно работают.
|
Именно аминоацил-тРНК-синтетазы ответственны за считывание генетической информации, которая записана в матричных РНК, поскольку они присоединяют каждую аминокислоту только к тем тРНК, у которых имеется соответствующий антикодон. Интересные идеи о том, как могла эволюционировать эта специфичность, формирующая генетический код. Но современные аминоацил-тРНК-синтетазы — это большие и сложные белки. Они прошли долгий эволюционный путь, который без системы программируемого синтеза белков не мог даже начаться. Получается как будто замкнутый круг: трансляция, как мы ее знаем сегодня, невозможна без аминоацил-тРНК-синтетаз, а аминоацил-тРНК-синтетазы не могли даже начать эволюционировать, пока не было механизма трансляции. Из этого, очевидно, следует, что в прошлом существовали более примитивные версии механизма трансляции, которые обходились без сложных белковых ферментов. Попытки найти простой и надежный способ неферментативного аминоацилирования РНК ранее уже предпринимались, но приносили лишь весьма скромные результаты. Как теперь выяснилось, главная проблема была в том, что исследователи использовали неоптимальные способы активации аминокислот. Химики из Университетского колледжа Лондона нашли удивительно простое и изящное решение этой проблемы. Они подумали, что все применявшиеся ранее способы активации аминокислот, возможно, просто слишком мощные для данной задачи. Реакционная способность молекулы оказывается слишком высокой, и она начинает реагировать со всем подряд. Исследователи использовали для активации аминокислот тиолы — сернистые аналоги спиртов (они несут SH-группу вместо OH-группы). Тиолы могут реагировать с аминокислотами, давая аминоацил-тиолы. Аминоацил-тиол — это тиоэфир аминокислоты и тиола с общей формулой R1-CH(NH2)-CO-S-R2 (например, на рисунок. изображен аминоацил-этантиол, у которого в качестве R2 — этильная группа CH2-CH3, а R1 — боковая цепь аминокислоты ). Использовать тиолы как средство переноса остатка кислоты (в данном случае аминокислоты), естественный способ решения данной задачи. В реальных биохимических процессах этот метод используется сплошь и рядом, чаще всего при помощи специальной вспомогательной молекулы с тиольной группой — кофермента А. Кофермент А есть у всех живых существ без исключения, а биохимические процессы с его участием явно старше последнего общего предка всех клеточных форм жизни (LUCA). Недавно, был открыт правдоподобный путь абиогенного синтеза пантетеина — самого главного, несущего тиольную группу компонента кофермента А Во многих ситуациях пантетеин и сам, без остальных частей кофермента, справляется со своими задачами. Оказалось, что аминоацил-тиолы охотно и очень избирательно реагируют с одиночными рибонуклеозидами, аккуратно сажая аминокислоту на «правильное» место, то есть на 2-й или 3-й углерод рибозы (гораздо реже — на 5-й). Ненужных побочных продуктов при этом образуется минимальное количество. Особенно важно, что аминоацил-тиолы практически не реагируют друг с другом и не дают случайных пептидов. Более того, аминоацил-тиолы, как выяснилось, не хотят реагировать даже с субстратами, похожими по своим свойствам на 2’,3’-OH рибозы — например, с глицеролом, у которого тоже есть ОН-группы, расположенные по соседству.
|